Concours de vulgarisation scientifique 2015 | lauréate
Le virus favorise le développement du cancer : mieux comprendre pour mieux guérir
En matière de cancer, la recherche scientifique s’intéresse de plus en plus à la possibilité que certains cancers soient causés par des virus. Ce nouveau champ d’étude est notamment exploré par Martin Bisaillon, professeur au Département de biochimie de la FMSS, et son équipe du Centre de recherche du CHUS qui tente d’identifier les mécanismes à l’origine de ce lien entre virus et cancer.
Présentement, le monde médical connaît plusieurs associations entre virus et cancer. L’association du cancer de l’estomac avec le virus d’Epstein-Barr, le virus responsable de la «mono» (mononucléose infectieuse), est connue. Aussi, un système de prévention a été mis en place pour la femme concernant le lien entre le virus du papillome humain (VPH) et le cancer du col de l’utérus, soit la vaccination Gardasil et le «pap» test (papanicolaou) régulier.
Les virus de l’hépatite B et l’hépatite C s’attaquent aux cellules du foie, les hépatocytes. Les hépatites qui en résultent peuvent mener jusqu’à un cancer du foie, le carcinome hépatocellulaire. L’équipe du Pr Bisaillon s’intéresse particulièrement aux mécanismes qui permettent aux virus de l’hépatite B et C de favoriser le cancer hépatocellulaire. Les recherches indiquent que ces virus sont redoutables pour leurs effets inflammatoires chroniques et destructifs des hépatocytes, mais aussi pour les mutations cellulaires cancérigènes. Même si le carcinome hépatocellulaire peut aussi exister sans infection à l’hépatite B ou C, les hépatites sont en cause dans 80% des cas¹.
Il faut d’abord exposer certains concepts génétiques afin de bien saisir le mécanisme par lequel un virus peut mener à un cancer. Tout d’abord, à l’exception des cellules reproductives, chaque cellule du corps humain comprend 23 paires de chromosomes. Chaque chromosome est composé de plusieurs centaines à des milliers de gènes. Les gènes sont des séquences d’ADN, et le génome, l’ensemble des gènes constitue notre patrimoine génétique.
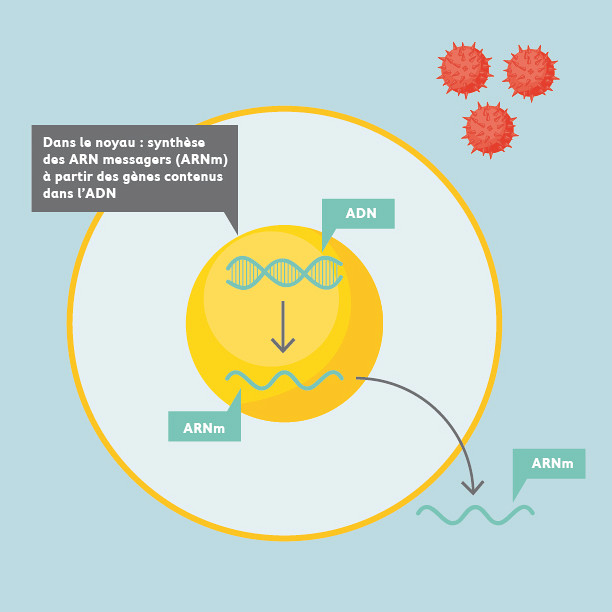
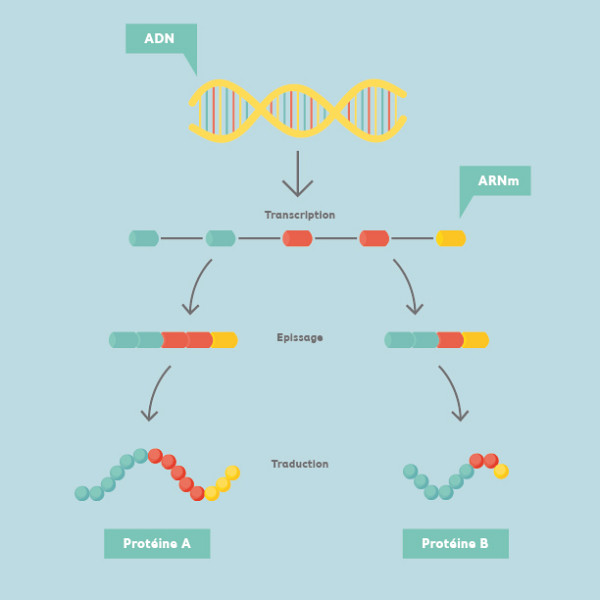
La cellule humaine est comparable à une petite usine de production de protéines. Le noyau, le centre de décision, contient l’ADN de la cellule. Un gène est lu comme un plan pour transmettre son information via l’ARNmessager (ARNm), qui est une copie de l’ADN. La copie de l’ADN en ARNm est un phénomène appelé la transcription. Une fois synthétisé l’ARNm est maturé. En fait, il subit un certain nombre de modifications, dont l’épissage qui consiste à éliminer certaines des régions qui le constituent, mais ceci de manière très précise en fonction de la protéine qui doit être produite à un moment précis ou à une condition spécifique. Ainsi, un ARNm pourra permettre de synthétiser différentes protéines en fonction des évènements d’épissage qu’il a subis. Finalement, l’ARNm sera lu à son tour comme un plan pour permettre la synthèse d’une protéine. Ce phénomène est appelé la traduction. Il y a une multitude de protéines différentes dans notre organisme, pensez aux anticorps, à l’hémoglobine dans notre sang ou encore à l’insuline bien connue pour être associée au diabète. Afin de pouvoir produire une panoplie de protéines, le corps a recours à des milliers de gènes ainsi que l’épissage alternatif. On appelle épissage alternatif la capacité de modifier un ARNm de façon à exprimer une grande variété de protéines avec différentes propriétés à partir d’un seul gène.
Certaines protéines créées par la cellule sont impliquées dans le contrôle cellulaire afin de limiter la présence de cellules avec des mutations et freiner leur multiplication. Certaines de ces protéines sont appelées facteurs de transcription et gènes suppresseurs de tumeur. Les facteurs de transcription permettent à l’ADN de transmettre les bons messages au reste de la cellule. Les gènes suppresseurs de tumeur empêchent la formation de cancer en contrôlant la multiplication cellulaire. Les gènes suppresseurs de tumeur agissent à titre de police et empêchent le chaos. Ces protéines permettent d’éviter la carcinogénèse, soit la formation de cancer. La carcinogénèse se base sur la multiplication de cellules anormales qui ne répondent pas aux facteurs de régulation des cellules. Les cellules tumorales perdent leur fonction et se multiplient pour finalement nuire aux cellules saines. Les protéines impliquées dans le contrôle cellulaire dépendent d’un épissage alternatif correctement régulé.
La capacité d’un virus hépatique à favoriser le cancer est en lien avec sa capacité à dérégler l’épissage alternatif de la cellule du foie. Le virus peut donc mener à la formation de protéines modifiées qui sont non fonctionnelles, ce qui peut entraîner la formation de cancer. L’équipe de recherche du Pr Bisaillon a démontré des modifications de l’épissage alternatif de 2500 gènes dans les cellules de carcinome hépatocellulaire, affectant ainsi les gènes suppresseurs de tumeur et les facteurs de transcription. En d’autres mots, l’infection virale a pour effet de modifier l’épissage alternatif de la cellule et ainsi, entraîne la production de toute une série de protéines différentes ce qui a pour effet de transformer la cellule normale en une cellule cancéreuse. L’étude menée par le Pr Bisaillon a même permis de démontrer qu’une protéine du virus de l’hépatite B (nommée HBx) a pour effet de modifier le mécanisme de l’épissage alternatif en soi, renforçant l’hypothèse de lien causal de l’hépatite B au cancer du foie.
Maintenant, le groupe du Pr Bisaillon désire approfondir comment l’infection virale modifie l’épissage alternatif en étudiant toutes les molécules et protéines impliquées dans ce mécanisme et ainsi mieux comprendre le développement du carcinome hépato-cellulaire. En termes de prévention de l’hépatite B, la vaccination est fortement recommandée à large échelle. En guise de traitement anti-cancéreux pour les personnes atteintes d’hépatite B ou C, l’équipe de recherche espère découvrir un type de médicaments qui permettrait de corriger les défauts de l’épissage alternatif causés par les virus et ainsi empêcher la formation de protéines altérées qui favorisent la prolifération de cellules tumorales et du cancer.